�й����������ڡ���Ӣ����ҽѧ��־���ϵ����ĵ�����ʲô��
ʱ�䣺2020-02-13 ����� �� ��Դ������� ���ߣ���ý�� - С + ��
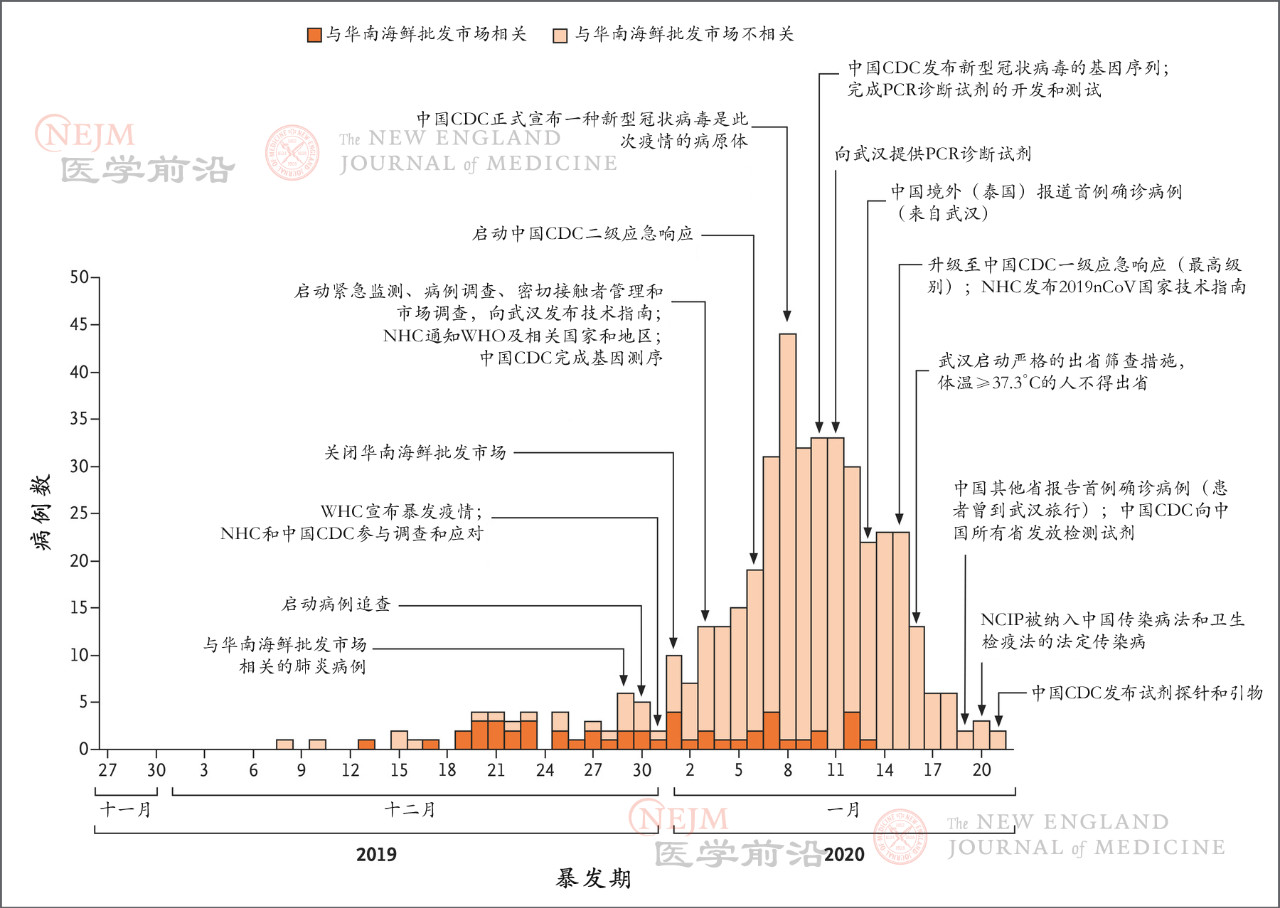
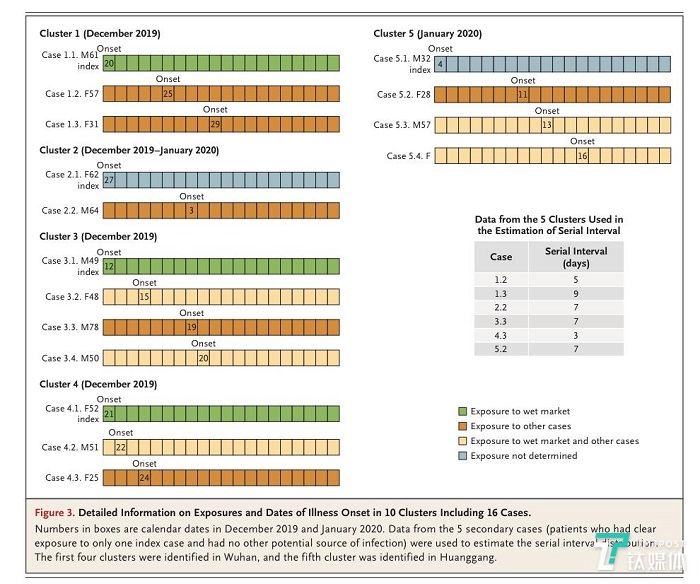
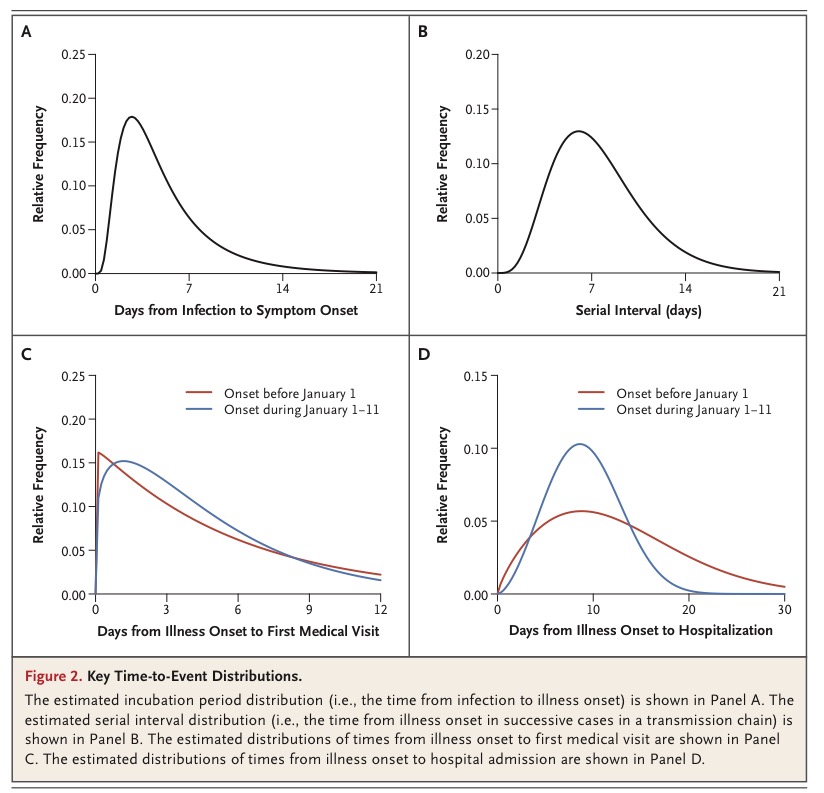
����ʱ��1 �� 30 �գ���������ҽѧ�ڿ�����Ӣ����ҽѧ��־�������������£��ԡ�����״������Ⱦ�ķ������й��人���ڴ�������ѧ��Ϊ�⣬ͨ�� 425 ���¹ڷ���ȷ�ﻼ�����ݣ��״���¶���� 1 �� 22 ���¹ڲ��������Ĺ��ɡ� �����������������Ϣ��ϸͼ ��Ϥ����ƪ���������й���������Ԥ�����ģ��³��й��������ģ�CDC��������ʡ�������ġ���۴�ѧ��γ�ҽѧԺ��������ѧԺ�ȶλ��ͬ��ɡ�������ý���������֣�����������������У������й������������θ߸����й��������ĸ����η��ӽ�������ʡ����������������ˣ����������Ŵ�ѧ��ҩ�����о������ص�ʵ���ҽ����Ծ����ڡ����ǰ�������ٰ칫�����Σ��������ʳ�P�����ָ��ֳ�����������۴�ѧ��γ�ҽѧԺԺ������ΰ���������صĿ�ѧ�ң���ν���״ηdz�Ȩ������Ϊ��ϸ���¹ڲ����������в�ѧ������¶�� ֵ��һ����ǣ��ڱ�ƪ�����ᵽ����ʵ�ϣ��� 2019 �� 12 ����Ѯ���¹ڲ��������нӴ���֮����ѷ����˼ʴ�����Ҳ������ν�ġ��˴��ˡ������⣬���������е�˵������ 2020 �� 1 �� 11 ��ǰ���Ѿ��� 7 ���人ҽ����Ա��Ⱦ������ ��һ��Ϣ����㷺�������й��������ľͱ��Ƶ��˷���˼⣬���ѷ����ɣ��Dz��� 12 ����Ѯ�����¹ڲ������˴��ˡ�֮���û�й������Լ�ȴ���ŷ����ģ� �Դˣ�1 �� 31 �գ��й���������������Ӧ�����Ķ��й��������Ļ�Ӧ�������ģ����в���������дǰ������ṫ���� һλ֪����ʿ�˵㽡�ű�ʾ�������ĵ��о��ͷ������ͺ�������Բ��������⣬Ҳ�ͺ�����Ϣ��������µó��ľ��ߡ�CDC ��̫��������֪�����˴��˵�����£��ڷ��ش�ʩ��������������һ�жϵľ��ߡ� ���й������������ڵķ��ؾ��ߣ��ǻ��ڶԲ�����չ�ε��жϣ��ǰ��չ�״������չ�ĵ�һ�������������ﴫ�˵������Ͻ��еģ�������ʵ�����¹��ѽ�չ���˴��˵ĵڶ��Ρ��� ���ܶԴ˻�Ӧ������۰��һ��������ƪ�����ڡ���Ӣ����ҽѧ��־�����������ᵽ�ĸ������ݲ�ʧΪһ���ô��ڸ����˽������¹ڲ����������ɵĴ��ڣ���ý��Ҳ�ݴ˸����������о������Լ����ڴ������IJ������⡣ ��μ�����������ѧ�ж������������һ���� ���ݼ�� ��ƪ�����ᵽ���¹ڷ�������IJ�����ͨ�����������ķ��ס����ӻ��Ƽ����ġ����ȣ���������� 4 ��������������Ϊһ��û�в���ԭ��ļ�����ҽ����Ϊ����Щ�����������±�: 1������(��38��C) 2������Ӱ��ѧ֤�� 3����ѭ���ٴ�ָ�Ͻ��п������� 3 �� 5 �������֢״���� 4�����������İ�ϸ�����ܰ�ϸ�������� Ϊ�˿���ʶ����ײ�������Ŭ��������ڷ��ֵ������ԣ��� 2020 �� 1 �� 3 �գ����������ƶ����������Ƶļ�ⷽ�����������ϵ��жϷ�����ʹ��֮��IJ������Ծ�����ҳ��������Լ�ȷ��DZ�ڵ��¹ڷ��ײ����� ���ڷ������Ʋ���֮�����й��������ij�Ա��ʡ���С��ؼ���ĵط�����Ԥ��������������������ֳ����в�ѧ�Ŷӣ����յ�֪֮ͨ��������ϸ���ֳ����飬���ռ��������걾���Ա����й��������IJ����о������м��м�⣬���ţ����й��������ĺ͵ط��������Ĺ�����Ա��ɵ������Ŷӣ����������ƺ�ȷ��� 2019-nCoV������״������������������ϸ���ֳ����飬ȷ����Ⱦ��Ⱦ�����Ʋ����� ͨ���ɷ��ܸ�Ⱦ�ߣ����ݣ�����ҽ����Ա�����нӴ��ߣ��������ռ������������С�ֵ��һ����ǣ��о���Ա�ڱ�Ҫʱ������ÿλ��Ⱦ���������������˷�̸������ͻ��ǰ�����ڵĽӴ�ʷ�������Ӵ�Ұ����������ڣ�ʱ�䣬Ƶ�ʺͷ�ʽ�������Ƿ��뻪�Ϻ��������г��й�����Ӵ�����¶���κ���ػ����¡����ң��о���ԱҲ��ȥ���飬�����й����������֢״�IJ����Ӵ�������Ϣ�����߷���ǰ 2 ������ȥ���ļ�ͥ�͵ط��ȡ� ���й��������ĵ������Ŷӣ�������춨λ����Ⱥ�壬���ƴ���Դ���жϴ���;�������ٴ����ʡ� �ڵ������ռ����������в�ѧ��Ϣ�������Ӵ�ʷ���¼�ʱ����ͽ�����ϵ�����ݣ��������в�ѧ��Ϣ��������Դ����Ϣ�����˽���˶ԡ�����һʽ���������������ݿ⣬��ͨ�� EpiData ������EpiData Association��������֤�� �������� ��Ը�Ⱦ����ԭ����ף�NCIP�������Ʋ�������������������֯��WHO���� 2003 ��� 2012 ��Ľ��飬�����ڷǵ� SARS ���ж������ۺ��� MERS �İ������д����ͽ���������⡣ ֵ��һ����ǣ�����δ֪���ײ�����Ҫ���������ĸ����� 1������,�������¼�¼; 2�����ķ���ѧ֤��; 3����ϸ�������ͻ��������ܰ�ϸ��������; 4�����ձ��ٴ�ָ�Ͻ��п�������3���֢״û�м��� ��������ȫ���������ķ��ײ��������߷���ǰ�������������뻪�Ϻ��������г������в�ѧ�Ӵ���������Լ��Ӵ�����������֢״���ߵķ��ײ��������Զ���Ϊ NCIP ����������ȡ�����䷶Χ�Ե����Ʒ��ײ���������Ҳ�����׳Ƶġ�Ⱥ���ԡ������� ������������������2020��1��18 �գ�һ���������ȷ�ﲡ��������Ϣ֮���������ڶ�����һ���Ʋ��������в�ѧ�±��� �ڷ���ǰ 14 ���ڳ��ַ��ջ���ֺ�����֢״���������人���У����������人�ˣ����ߣ������нӴ��ߡ� ����ȷ�ﲡ���Ķ���Ϊ��ͨ���������ַ����е�һ�������ں������걾�м�����״������2019-nCoV�������ԣ�Ҳ����������Ժʿ��˵�ġ������ӡ����Լ��м�ⷽ�����ſ���ȷ� 1�������2019-nCoV�� 2��ʵʱ��ת¼�ۺ�ø����Ӧ(RT-PCR)������������ʾ2019-nCoV���ԣ� 3��������2019-nCoVƥ��Ļ������С� ʵ���Ҽ�� ����״����ʵ���Ҳ��Է��������� WHO ��ǰ�Ľ��飬ȡ�������ϡ��º������걾����ȡ RNA �걾����ʹ�����人�����о��������Ƴ��� 2019-nCoV �����������̽�룬����ȷ���ͨ��ʵʱ RTPCR ���в��ԡ� �������ں���ʡ�������ĵ����ﰲȫ������ʩ�н��еģ�Ȼ�����й��������ĵĹ��Ҳ������������о�����������ˡ� ��������б�ͨ���ض���ʵʱ RT-PCR ���Ϊ���ԣ�����Ϊ�ò�������ʵ����ȷ�ϡ���С�� 37 ��ѭ����ֵ��Ct ֵ������Ϊ���ԣ������ڵ��� 40 �� Ct ֵ����Ϊ���ԡ�Ct ֵ����Ϊ 37 �� 40 �ģ�����Ϊ�е���������Ҫͨ�����²��Խ���ȷ�ϡ� �������֮��Ct ֵС�� 40�����ҹ۲쵽���Եķ�ֵ�������¼��Ϊ���ԡ� ͨ�����ַ���֮һ���ӻ��ߵ�֧���ܷ��ݹ�ϴҺ�����м����������飺Sanger ����Illumina ��������ײ������й�����Ԥ������������ǿ�����ﰲȫʵ������ʩ�У����������걾���ֵ�ϸ���н��в������롣 ͳ�Ʒ��� ���ݷ������ڻ����������ߣ����������в�ʶ��Ϳ����йش�ʩ�Ĺؼ����ڣ�����������������Ե�ɡ��������������������˿�ͳ��ѧ������ �Լ���¶���������������ߵ�״����ͨ��������̬�ֲ������DZ���ڷֲ������Ӹ�Ⱦ��������ʱ���ӳ٣��Լ���¶ʷ���������ڵ�����(��һ���ֲ����о��п��õ���ϸ��Ϣ)�����״ξ������Ժ����IJ�����Ϣ������ Weibull �ֲ���ϣ��������������Ŷӵľۼ���������ݣ�������������ϣ�����٤���ֲ����������м���ֲ������¾��嶨�壬�����������������м�����������֮����ӳ٣������Ʋ�ȷ���¹ڲ����Ĵ������봫����Χ�� ���⣬��һͳ��ͼ�����Ƿ��� 12 �� 10 ���� 1 �� 4 ���ڼ䷢����������������������������ٶȣ�Ԥ���� 12 �� 13 ���人������ʽ����֮���ֵĸ�Ⱦ�������ܿ����ӣ�������������Ⱦ�ķ�������ģ��(ʹ�ø��·���ʽ���� ��)��ȷ���뻪�Ϻ���Ʒ�����г��Ƿ��з�����������������ʹ�ô�ģ�����ó����в��������ʣ����в��ı���ʱ��ͻ�����ֳ��( R0)�� ���� SARS �ڼ�� R0 ��ֵ����ƽ��ֵΪ 8.4������Ϊ 3.8�����ж��¹ڲ����Ĵ����Ƿ�� SARS ��ǿ�������Ƿ��ǿ�ҡ� ��������ʹ�ô����ݣ���MATLAB ����(MathWorks)��DZ���ڣ� ���м�����������ʺ� R0 ���з�����ʹ�� SAS ����(SAS Institute)�� R ����(R Foundation for Statistics Computing)�����˾�������� ���ݽ�����������Ի��߸���Ⱦ�¹ڲ��� ���������н��ͣ����в��ķ����Ǹ��Ų�����ָ�����������������½��ܿ��������ڶ���������IJ����IJ�ȷ�����Լ������ͱ�����ӳ٣������Ƿ����ʵ������յ㡣 �����ᵽ�����ݣ���ʾ12�¾ͷ������˼�֮�䴫�� �dz���Ҫ���ǣ���ͼ���ߵĺ�벿�ֲ�����ʾ�¼����������������٣��������ڽ�ֹ����֮ǰȷ ��������ʱ���Ƴ��ˡ����ǵ�����ʱ������ƣ�����Լ��еĿ����Ժ�ʹ���������ӣ� ����ڽ��� 1 �·ݲ��������ٶ�ʱӦ����С�ġ� ͨ�����人�н��� 1��22�գ���425���¹ڷ���ȷ�ﻼ�߽��з������֣�������λ����Ϊ 59 �꣨��ΧΪ 15 �� 89 �꣩��56% Ϊ���ԣ��� 240 ����15 �����µĶ�ͯû�����ڲ������ܵ���˵���������Ի��߸���Ⱦ�¹ڲ��������Ҹ��п����ڻ��Ϻ��������г��й��Ӵ��� ���¹ڷ��IJ�����������ͳ�� �����Ŷӻ������ĵ��У��Խ���Ŀǰ�IJ���ʱ������˷��������������ڴ����Σ� ��һ��������� 1 �� 1 ��(�����Ϻ��������г��ر�)֮ǰ�����Ļ��ߣ� �ڶ������Ƿ���ʱ��Ϊ 1 �� 1 ���� 1 �� 11 �յĻ��ߣ��������人�ṩ RT-PCR �Լ������ڡ�������������Щ�� 1 �� 12 �ջ�֮�����ˡ� ��������ʱ���У�ҽ����Ա�еIJ������������ӡ� �����ڱ����ĵ�ͼ�����Լ�ժҪ�����б������� 2019 ��12����Ѯ���������нӴ���֮���ѷ����˼ʴ��������������е�һ��ͼ�������������IJ����������˻��Ϻ��������г���¶ʷ������12�µ�ʼ���뻪�Ϻ����г�����صIJ������ָ������������֮�����Ƿ����人�ֽε��¹ڷ��ײ�������ʱ��ԼΪ 7.4 �졣���нӴ���֮����˼ʴ����� 12 ����Ѯ��ʼ�Ѿ����������ڴ˺�һ��������ɢ���� ���ڲ�����¶���ݷ����������ᵽ��������Ա��� 10 ��ȷ�ﲡ���ı�¶���ݣ�����ƽ��DZ����Ϊ 5.2 �죨95% �������䡾CI��4.1 �� 7.0���ֲ��ĵ� 95 ���ٷ�λ�� 12.5 �죨95% CI��9.2 �� 18)������ͨ����õ� 5 ����������Ϣ�Է���ʱ��ȷ�������Ʋ������м���ֲ���ƽ��ֵ(��SD)Ϊ 7.5��3.4 �죨95%CI��5.3 �� 19)�� �й�10����Ⱥ(����16������)�ı�¶�ͼ����������ڵ�������Ϣ ����˵�������¹ڲ�����DZ���ڣ�����ƽ�� 10 �����ң�Ҳ����֮ǰ�й������������µ�˵����DZ����������3�죬�����14�죬������ӡ�ȿ챨�����ù���������˵������һDZ�����ʱ�䣬������ 28�����ң���ֹ�ٴδ����� �ڽ��� 2020 �� 1 �� 4 �յ����������У���Ⱦ��������Ϊÿ�� 0.10(95% CI��0.050~0.16)������ʱ��Ϊ 7.4 ��(95% CI��4.2~14)��Ӧ��������һ�˴�����һ�˵ļ��ʱ��ֲ���������� R0 Ϊ 2.2(95% CI��1.4~3.9)�� ��1��1��֮ǰ������ 45 �������У��ӷ������״ξ����ƽ������ڹ���Ϊ 5.8 ��(95% CI��4.3~7.5)����1 �� 1 �պ� 1 �� 11 ��֮��� 207 �������Ļ������ơ�ƽ��Ϊ 4.6 ��(95%CI��4.1 �� 5.1)���ҡ��Ӷ�˵�����������鱻�㷺���������ҽ��з��ش�ʩ���������Ļ��߲�û�мӿ��������ȡ� �ؼ����鷢����ʱ��ֲ�����ͳ�� ��1��1��֮ǰ������ 44 �������У��ӷ�����סԺ��ƽ������ڹ���Ϊ 12.5 ��(95% CI��10.3��~14.8)����һ����ڳ���1��1����1��11���ڼ䷢����189�����ߣ���ֵ��9.1�죻95% CI��8.6~9.7���� �����Ŷӳƣ���ͼ�����У�û��Ϊ 1 �� 12 �ջ�֮���Ļ�������Щ�ֲ�ͼ����Ϊ��δ������Щ���ڷ����Ҳ��̽ϳ��Ļ��ߡ� ��Ϥ����������ݱ����У��й��������ġ���۴�ѧ�������Ŷӳ�Ա���ṩ�� NCIP ��������ѧ�����в�ѧ�����ij������������������״ι�֮���ڡ� ��������Ϊ�����ڴ���ģʽͨ������չʾ�����ˣ��Խ�����ȫ����¹ڷ��ķ��ع����������ڱס� ���ĵ�ַ�� https://www.nejm.org/doi/pdf/10.1056/NEJMoa2001316?articleTools=true ���������ᵽ��������Ϣ�� 1��The 2019-nCoV Outbreak Joint Field Epidemiology Investigation Team, Li Q. Notes from the field: an outbreak of NCIP (2019-nCoV) infection in China �� Wu- han, Hubei Province, 2019�C2020. China CDC Weekly 2020;2:79-80. 2. Tan WJ, Zhao X, Ma XJ, et al. A novel coronavirus genome identified in a clus- ter of pneumonia cases �� Wuhan, China 2019�C2020. China CDC Weekly 2020;2:61-2. 3. ZhuN,ZhangD,WangW,etal.A novel coronavirus from patients with pneumonia in China, 2019. N Engl J Med 2020 January 24 (Epub ahead of print). 4. Xiang N, Havers F, Chen T, et al. Use of national pneumonia surveillance to de- scribe inf luenza A(H7N9) virus epidemi- ology, China, 2004�C2013. Emerg Infect Dis 2013;19:1784-90. 5. Munster VJ, Koopmans M, van Doremalen N, van Riel D, de Wit E. A novel coronavirus emerging in China �� key questions for impact assessment. N Engl J Med. DOI: 10.1056/NEJMp2000929. 6. WHO guidelines for the global sur- veillance of severe acute respiratory syn- drome (SARS). 2004 (https://w w w.who .int/csr/resources/publications/WHO _CDS_CSR_ARO_2004_1.pdf?ua=1). 7. Middle East respiratory syndrome case definition for reporting to WHO. 2017 (https://www.who.int/csr/disease/ coronavirus_infections/mers-interim-case -definition.pdf?ua=1). 8. Azhar EI, El-Kafrawy SA, Farraj SA, et al. Evidence for camel-to-human trans- mission of MERS coronavirus. N Engl J Med 2014;370:2499-505. 9. New coronavirus pneumonia prevention and control program (2nd ed.) (in Chinese). 2020 (http://www.nhc.gov.cn/jkj/s3577/ 202001/c67cfe29ecf1470e8c7fc47d3b751e88 .shtml). 10. Laboratory diagnostics for novel coro- navirus. WHO 2020 (https://www.who.int/ health-topics/coronavirus/laboratory -diagnostics-for-novel-coronavirus). 11. Lipsitch M, Cohen T, Cooper B, et al. Transmission dynamics and control of severe acute respiratory syndrome. Sci- ence 2003;300:1966-70. 12. Bauch CT, Lloyd-Smith JO, Coffee MP, Galvani AP. Dynamically modeling SARS and other newly emerging respiratory ill- nesses: past, present, and future. Epide- miology 2005;16:791-801. 13. Paules CI, Marston HD, Fauci AS. Coronavirus infections �� more than just the common cold. JAMA 2020 January 23 (Epub ahead of print). 14. Perlman S. Another decade, another coronavirus. N Engl J Med. DOI: 10.1056/ NEJMe2001126. 15. de Wit E, van Doremalen N, Falzarano D, Munster VJ. SARS and MERS: recent insights into emerging coronaviruses. Nat Rev Microbiol 2016;14:523-34. 16. WongG,LiuW,LiuY,ZhouB,BiY, Gao GF. MERS, SARS, and Ebola: the role of super-spreaders in infectious disease. Cell Host Microbe 2015;18:398-401. 17. Chan JF, Yuan S, Kok KH, et al. A fa- milial cluster of pneumonia associated with the 2019 novel coronavirus indicating person-to-person transmission: a study of a family cluster. Lancet 2020 January 24 (Epub ahead of print). 18. Wu P, Hao X, Lau EHY, et al. Real- time tentative assessment of the epide- miological characteristics of novel coro- navirus infections in Wuhan, China, as at January 2020. Eurosurveillance 2020; 25(3):pii=2000044. 19. Lipsitch M, Hayden FG, Cowling BJ, Leung GM. How to maintain surveillance for novel influenza A H1N1 when there are too many cases to count. Lancet 2009; 374:1209-11. |